김형기 교수팀, 암줄기세포 분화 이용한 종양치료법 제시
뇌종양 등 암의 맞춤형 항암제 개발 기대, 국제학술지 Clinical Cancer Research 논문 게재

▲ 생명과학대학 생명공학과 김형기 교수
생명과학대학 생명공학과 김형기 교수 연구팀이 암줄기세포의 줄기세포능을 억제하기만 할 것이 아니라 분화를 유도하는 새로운 종양치료 전략을 제시해 화제다.
* 암줄기세포(Cancer stem cell) : 성체줄기세포와 유사하게 자기재생과 분화능력을 가진 소수의 암세포
* 줄기세포능(stemness) : 여러 종류의 세포로 분화할 수 있는 능력
* 분화(differentiation) : 미숙한 세포에서 특정 기능을 갖는 세포로의 변화
이번 연구 성과는 과학기술정보통신부․한국연구재단 기초연구지원사업 (개인·집단연구) 지원으로 수행됐으며 국제학술지 임상종양연구(Clinical Cancer Research) 12월 12일 논문으로 게재됐다.
- 논문명 : Inhibition of ID1-BMPR2 intrinsic signaling sensitizes glioma stem cells to differentiation therapy
- 저 자 : 김형기 교수(교신저자, 고려대학교), 김웅 박사(제1저자, 고려대학교), 전희영(공동저자, 고려대학교), 김은정(공동저자, 고려대학교), 김준겸(공동저자, 고려대학교), 이선용(공동저자, 고려대학교)
대부분의 종양조직에서 발견되는 암줄기세포는 암의 발생, 전이의 원인이다. 또한 방사선 항암치료의 내성이 강해서 암을 재발시킨다. 최근 암줄기세포를 표적으로 삼는 종양치료법이 연구되고 있지만, 암줄기세포의 줄기세포능을 억제하였을 때 항암 효과가 미미하거나 암이 재발되는 등 한계가 있었다.
연구팀은 암줄기세포의 분화유도 과정을 규명하고, 줄기세포능을 억제하는 동시에 분화능력을 촉진하는 일종의 ‘채찍과 당근’ 치료 전략을 제시했다. 연구 결과, 전사조절인자인 ID1이 줄기세포능과 분화능력을 모두 조절한다는 것이 확인됐다. ID1은 윈트(WNT)와 소닉헷지호그(SHH) 신호전달계를 활성화하여 줄기세포능을 촉진시키고 BMP 신호전달계를 억제하여 분화를 억제했다.
* ID1 : 줄기세포의 분화를 억제하는 인자로서, 정상조직보다 뇌종양에서 많이 발현됨.
반대로 조절하여, 뇌종양줄기세포에서 윈트와 소닉헷지호그 신호를 억제하고 BMP 신호를 활성화시키면 뇌종양에 걸린 생쥐의 생존율이 증가했다. 뇌종양줄기세포의 분화 유도를 통한 항암치료 가능성을 입증한 것이다.
김형기 교수는 “이 연구는 암줄기세포의 분화조절 과정을 규명하고, 줄기세포능과 분화유도능을 표적으로 하여 종양을 억제하는 새로운 ‘항암분화치료’ 전략을 제시한 것”이라며 “다양한 종류의 암줄기세포에 대한 맞춤형 항암제 개발의 기술적 진보가 기대된다”라고 연구의 의의를 설명했다.
[ 용 어 설 명 ]
1. 암줄기세포 (Cancer stem cell)
○ 거의 모든 암에서 발견되는 정상적인 줄기세포와 유사한 자기 재생과 분화능력 특징을 갖고 있는 소수의 암세포로서 줄기세포 능력이 없는 일반 분화된 암세포와 다르게 이들 암줄기세포만이 종양을 형성할 수 있으며, 특히 전이 및 항암치료 후 재발 원인이 되는 세포로 알려져 있다.
2. 줄기세포능(stemness)
○ 여러 종류의 세포로 분화할 수 있는 능력
3. 분화(differentiation)
○ 미숙한 세포에서 특정 기능을 갖는 세포로의 변화
4. ID1 (Inhibitor of Differentiation 1, 분화억제인자1)
○ 헬릭스-루프-헬릭스(Helix-Loop-Helix) 구조를 가지며 DNA 결합능력이 없는 단백질로서 DNA 결합능력이 있는 헬릭스-루프-헬릭스 구조를 가진 다른 전사인자(transcription factor)와 결합하여 유전자 전사(transcription)을 억제하는 작용을 한다. 보통 세포 분화를 유도하는 전사인자들을 억제하여 세포 분화를 억제하고, 줄기세포 능력을 유지하도록 하는 기능이 알려져 있다.
5. BMP(Bone morphogenetic protein, 뼈형태형성단백질)
○ 일반적으로 줄기세포의 분화를 유도하는 신호전달체계로 알려져 있다. BMPR2는 BMP receptor II이다.
6. 종양구체 형성능력
○ 암줄기세포를 생체 외 배양하면 나타나는 특성 중 하나로, 일반적인 암세포는 배양용기 밑바닥에 부착하여 자라야 하는 반면 암줄기세포는 특정 배양액에서 배양하면 액체 속에 부유하여 구체를 형성하면서 자라는 능력을 말한다.
7. Myc
○ 강력한 종양유발인자로 알려져 있으며 다양한 암에서 높은 발현량으로 발견되고 있다.
8. miRNA17/20a
○ microRNA의 일종으로 종양을 촉진한다고 알려져 있다.
9. 교모세포종 (Glioblastoma)
○ 교모세포종은 4등급의 신경교종으로 신경교종 중에서 가장 악성이며 조직학적으로는 역형성 성상 세포종에 괴사소견이 추가된 것입니다. 이 종양은 가장 흔한 악성 원발성 뇌종양으로 성인 신경교종의 1/4, 소아 신경교종의 15%를 차지하며 진단 치료 후 평균 생존율이 14개월 이내인 악성 종양이다.
10. 신호전달계 (signaling pathway)
○ 세포 외부의 특이적인 신호나 변화를 세포막 수용체가 인지하여 세포 내 단백질들의 체계적이고 역동적인 변화를 일으켜 세포의 특성 유지과 기능을 수행하는 과정에 관여하는 이들 분자 간의 상호 연결과 역동적인 변화를 의미한다.
[ 그 림 설 명 ]
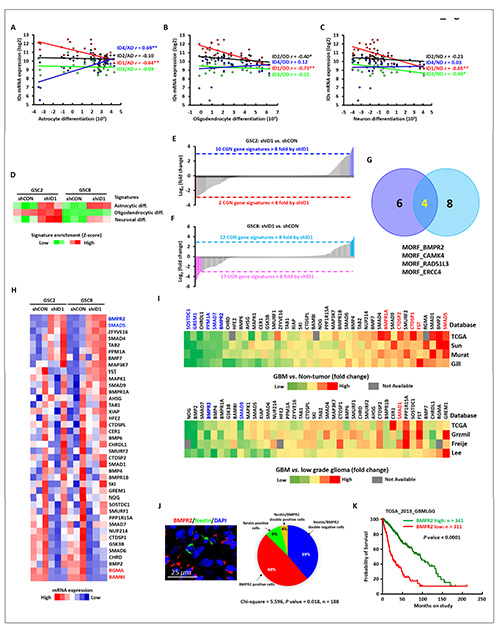
(그림1) 생물정보학적 방법으로 ID1이 BMPR2를 통하여 뇌종양줄기세포의 분화를 조절한다는 것을 확인했다.
(A-C) 공개된 데이터에서 ID family 중 유일하게 ID1이 세 가지 lineage로의 분화신호와 부의 상관관계를 보여주는 것을 확인했다.
(D) 실험실에서 구축된 뇌종양줄기세포주에서도 A-C에서 확인한 내용을 확인했다.
(E-H) ID1이 감소되었을 때 BMPR2 유전자가 가장 많이 증가되었다는 것을 확인했다.
(I) 공개된 여러 종류의 데이터에서 BMPR2가 교모세포종에서의 발현량이 정상조직에 비해, 그리고 낮은 grade의 뇌종양에 비해 모두 낮다는 것을 확인했다.
(J) 뇌종양 환자조직에서 BMPR2를 발현하는 분화된 세포와 줄기세포 표지인자인 Nestin을 발현하는 미분화된 줄기세포를 면역염색법으로 확인했다.
(K) 공개된 데이터에서 BMPR2의 발현에 따라 뇌종양환자의 생존율을 비교 분석했다. 결과 BMPR2의 발현이 낮은 뇌종양환자들의 예후가 훨씬 안 좋은 것을 확인했다.
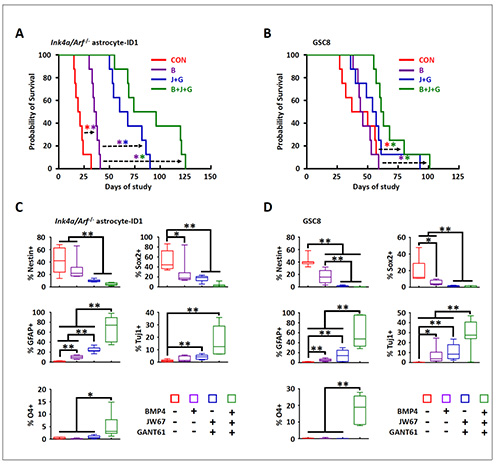
(그림2) 마우스 실험을 통하여 항암분화치료 전략을 확인
(A-B) 두 가지 ID1을 발현하고 있는 뇌종양줄기세포를 이식하여 악성뇌종양을 가진 마우스는 줄기세포능 억제제(J, G)와 분화유도제(B)를 동시에 처리했을 때 그 예후가 가장 좋은 것을 확인했다.
(D) 실험 후 마우스의 뇌종양 조직을 추출하여 면역화학법으로 줄기세포 표지인자와 분화세포 표지인자를 확인했다. 결과 세 가지 약물을 모두 처리했을 때 줄기세포 표지인자(Nestin, Sox2)가 대조군에 비해 현저히 감소하는 것을 확인했고, 분화세포 표지인자(GFAP, Tuj1, O4)는 현저히 증가하는 것을 확인했다.
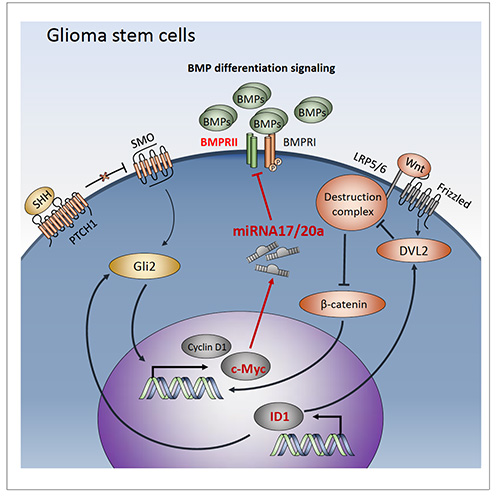
(그림3) 암줄기세포 항암분화치료 전략 제시
ID1 전사조절인자가 WNT/SHH 줄기세포 조절신호를 통하여 Myc, miRNA-17/20a의 발현을 높여주고 이로써 분화유도신호인 BMP를 억제한다는 것을 밝혔다. 실험을 통하여 줄기세포 조절신호를 억제하고 분화유도신호를 활성화 시키면 암줄기세포가 억제되면서 종양도 억제되는 것을 확인함으로서 암줄기세포 항암분화치료 전략을 제시했다.
커뮤니케이션팀 서민경(smk920@korea.ac.kr)