“종양 내 이질적 환경을 동시 표적하는 항암전구약물 개발” 화제
김종승·지성길 교수팀 연구결과, 화학분야 국제학술지 JACS 표지 논문으로 게재돼

▲ 윗줄 왼쪽부터 Amit Sharma 박사, 이민구 박사, 원미애 박사
아랫줄 왼쪽부터 구세영 박사, 지성길 교수, 김종승 교수
화학항암제 및 표적항암제를 비롯한 기존의 항암 치료 방식의 한계를 극복할 수 있는 항암전구약물 전달 기술이 국내 연구진에 의해 개발됐다.
이과대학 화학과 김종승 교수, 생명과학대학 생명과학과 지성길 교수, Amit Shama 박사, 이민구 박사, 원미애 박사, 구세영 박사 공동 연구팀은 “종양 내 이질적인 환경에서 동시에 약물이 활성화되어 기존 항암제의 부작용은 줄이면서 항암효과는 극대화 할 수 있는 새로운 항암표적치료기술을 개발했다.”고 밝혔다. 이에 따라 향후 새로운 방식의 항암치료기술 개발에 대한 기대가 높아지고 있다.
암은 역동적인 질환으로 발병하여 진행되는 동안 이질성을 갖게 된다. 종양이질성(Tumor heterogeneity)은 동일 암종(Inter-tumor), 또는 한 종양 내(Intra-tumor)에서 종양 세포들의 생물학적 특성이 서로 다른 것을 의미하며, 종양의 발생·증식과정, 대사과정, 유전자 발현 등의 여러 요인이 축적되어 나타난다. 다양한 유전적 변이는 종양세포 별 상이한 단백질 발현을 유도하고, 이에 따라 세포의 주요 에너지대사과정과 같은 세포생물학적 특성이 달라진다. 종양이질성은 한 가지 치료 방법으로 모든 종양세포를 동시에 치료할 수 없게 만들어 종양 재발(Tumor recurrence)의 한 원인으로 대두되고 있다.
발암과 악성화 과정에서 일어나는 다양한 유전자 변이와 손상, 비정상적인 상태에서 무분별하게 일어나는 세포 복제 및 분열은 활성산소(Reactive Oxygen Species)를 과발현시킨다. 이러한 산화적 스트레스(Oxidative stress)가 축적되면, 일반적으로 세포자살경로(Cell apoptosis)에 의해 세포가 사멸하게 된다. 그러나 종양세포는 산화적 스트레스를 무력화 시킬 수 있는 항산화시스템(Antioxidant system)을 과발현시켜 산화/환원적 환경에 밸런스를 유지하며 생존한다. 따라서 모순적이게도 종양 내에는 정상세포보다 산화적 스트레스가 높거나 혹은 항산화시스템이 과 발현된 종양세포가 공존하는 이질적인 환경이 조성된다.
이번 연구의 화합물은 항암제인 SN-38, 대장암을 선택적으로 표적할 수 있는 사이클로옥시게나제-2 (Cyclooxygenase-2:COX-2) 억제제 그리고 활성산소의 일종인 과산화수소 (Hydrogen peroxide:H2O2)와 대표적인 항산화시스템의 일종인 글루타치온(Glutathione: GSH)에 의해 항암제가 활성화 되는 약물전구체로 구성돼있다. 따라서 이번 연구의 화합물은 대장암에 선택적으로 축적되어 정상세포를 회피하여 약물을 전달할 수 있을 뿐만이 아니라 산화/환원 스트레스가 내재된 이질적인 종양세포환경에서 각각 활성화됨으로서 약물이 동시에 방출되어 항암효과를 극대화 시킬 수 있다. 또한 사이클로옥시게나제-2(COX-2)를 억제함으로서 종양 내 염증반응을 낮추어 정상적인 면역기능의 활성화가 촉진됐다.
이번 연구에서 개발된 종양이질성 표적 항암전구약물을 인간유래의 대장암 세포가 이식된 마우스 종양모델에 투여한 결과, 대조군의 40배 이상, SN-38 투여 군에 비해 2배 가까이 종양 부피가 감소됨을 확인했으며 또한 특이적 약물부작용도 나타나지 않았다.
공동 연구팀은 종양이질성의 특성을 이해하고, 종양 이질적 환경에서 동시표적 가능한 항암전구약물을 합성하여 대장암 선택적 약물의 효능이 향상된 새로운 항암표적치료제를 개발하는데 성공했다. 김종승·지성길 교수는 “종양이질성 신규 항암표적치료제를 통해, 암세포들의 환경적 차이를 이해하여 종양의 이질성 및 다양성의 치료한계를 극복하고 치료의 효율성을 높인 선택적 항암표적약물 치료전략을 활용하여, 향후 암 치료제 개발 분야에 큰 도움이 될 것으로 기대한다.”고 밝혔다.
연구 결과는 화학분야 국제학술지 “JACS (Journal of the American Chemical Society)”에 2019년 10월 2일 논문으로 게재됨과 동시에 10월호 대표 표지 논문으로 선정되는 쾌거를 거뒀다.
* 논문명 : Targeting Heterogeneous Tumors Using a Multifunctional Molecular Prodrug
(종양 내 이질적 환경을 동시 표적하는 항암전구약물 개발)
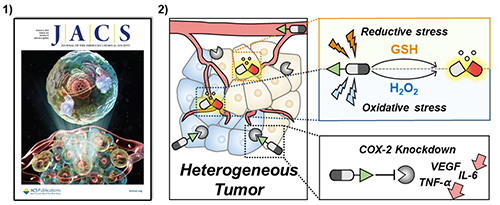
▲ 그림설명 : 종양 내 이질적 환경을 동시 표적하는 항암전구약물개발
1) JACS 2019년 10월호 표지 논문으로 선정.
2) 과산화수소(Hydrogen peroxide)가 과발현된 산화적 스트레스(Oxidative stress)환경과 글루타치온(GSH)이 과 발현된 환원적 스트레스(Reductive stress)환경에서 동시에 항암제가 활성화 되어 암 세포사멸을 유도함. 사이클로옥시게나제 2(COX-2) 억제제에 의해 대장암을 표적하며 VEGF, IL-6, TNF-α와 같은 염증관련 물질의 생성을 억제하여 항암효과를 높임.